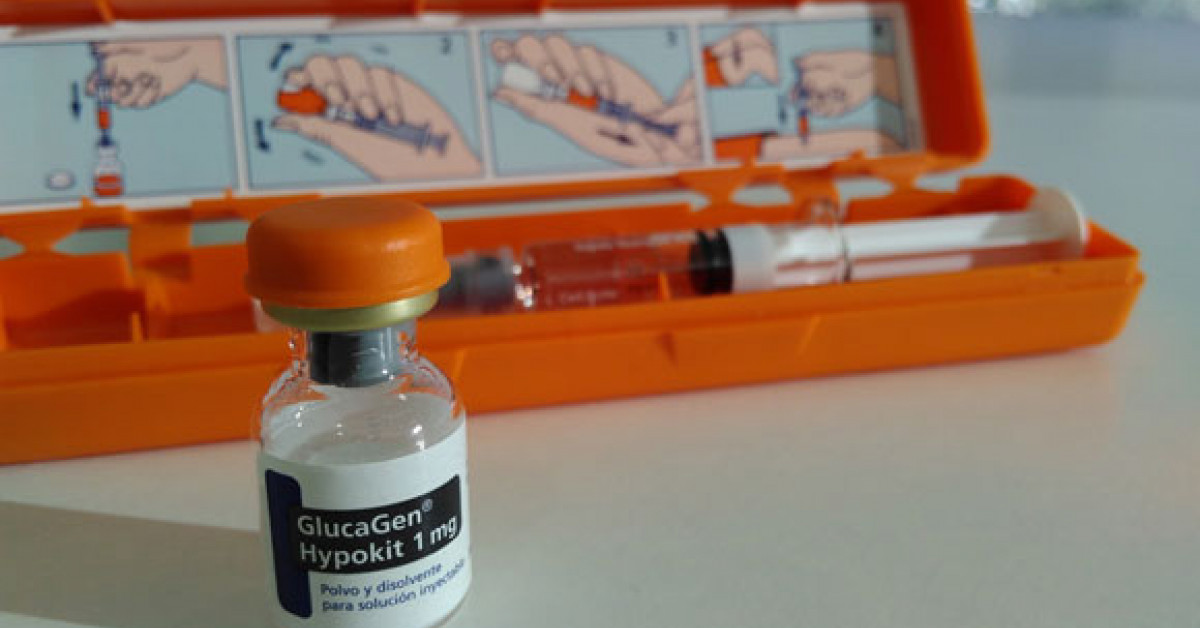
Como un avance considerable en términos de salud, la FDA (Administración de Drogas y Alimentos de Estados Unidos) ha aprobado el primer fármaco para tratamiento de hipoglucemia grave. Se trata del primer genérico de glucagón inyectable USP 1mg/vial empaquetado en un kit de emergencia. Está indicado, además, como ayuda de diagnóstico en el examen radiológico del estómago, el duodeno, el intestino delgado y, también, el colon cuando sería ventajosa una motilidad intestinal reducida.

¿Qué es la hipoglucemia grave?
Cuando se habla de hipoglucemia grave se hace referencia al momento en que el azúcar en sangre de una persona cae a niveles en que se confunde o puede llegar a perder el conocimiento. También pueden darse otros síntomas. Se trata de casos en los que se necesita de un tratamiento eficaz. En general, es algo que aparece mayormente en personas con diabetes que utilizan un tratamiento con insulina.
Glucagón genérico para hipoglucemia
El glucagón genérico para inyección se trata de una versión sintética del glucagón humano. Es una hormona que se encarga de que el hígado aumente rápidamente los niveles de azúcar en sangre. Además, es una hormona que ralentiza el movimiento del tracto gastrointestinal. Los efectos secundarios que se suelen asociar al uso del inyectable son vómitos y náuseas, como así también enrojecimiento, hinchazón en la zona de inyección y, además, un aumento temporal de la frecuencia cardíaca.
Sally Choe, directora de la Oficina de Medicamentos Genéricos en el Centro de Evaluación e Investigación de Medicamentos de la FDA, explica que:
“El uso de glucagón inyectable ha sido aprobado para su uso en los EE. UU. Durante más de 20 años, pero hasta el día de hoy, no ha habido un genérico aprobado de este importante medicamento que pueda salvar la vida de personas que pueden experimentar la condición grave de niveles muy bajos de azúcar en sangre (…) La aprobación de hoy refleja el compromiso continuo de la FDA de promover el acceso de los pacientes a productos farmacéuticos genéricos de alta calidad y menor costo que sean tan seguros y efectivos como sus contrapartes de marca. Apoyar el desarrollo y ampliar las oportunidades para llevar al mercado copias genéricas de medicamentos complejos, como el glucagón, ha sido un enfoque importante de nuestros esfuerzos para mejorar la competencia y ayudar a reducir los precios de los medicamentos”.
Actividades de la FDA

La FDA mantiene una lista de productos farmacéuticos sin patente ni exclusividad sin un genérico aprobado para mejorar la transparencia. Además, para lograr alentar el desarrollo y la presentación de solicitudes de medicamentos que cuentan con competencia limitada. En este sentido, el glucagón se encuentra en dicha lista. También se otorga prioridad a la revisión de las presentaciones de medicamentos genéricos para los que hay menos de tres genéricos aprobados en el listado de referencia.
FDA toma medidas con regularidad para ayudar a guiar a la industria a través del desarrollo de medicamentos genéricos. El desarrollo de estos productos puede ser más difícil por su complejo ingredientes activo o su modo de administración. Por eso, muchos medicamentos complejos no cuentan con competencia genérica incluso luego de que las patentes y las exclusividades ya no bloqueen la aprobación de genéricos.







Comment here