El día 11 de diciembre de 2020, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha autorizado la primera vacuna contra el covid-19 para su uso de emergencia. Se trata de la vacuna de Pfizer en asociación con BioNTech, para su distribución en los Estados Unidos. Esta autorización es considerada como un hito fundamental para luchar contra la pandemia del coronavirus. Pandemia que ha afectado a tantas personas, especialmente en el país de América del Norte.
 En este sentido, explica la FDA que:
En este sentido, explica la FDA que:
“La FDA ha determinado que la vacuna Pfizer-BioNTech COVID-19 ha cumplido con los criterios legales para la emisión de una EUA. La totalidad de los datos disponibles proporciona evidencia clara de que la vacuna Pfizer-BioNTech COVID-19 puede ser eficaz para prevenir el COVID-19. Los datos también respaldan que los beneficios conocidos y potenciales superan los riesgos conocidos y potenciales, lo que respalda el uso de la vacuna en millones de personas de 16 años o más, incluidas las personas sanas. Al tomar esta determinación, la FDA puede asegurar al público y a la comunidad médica que ha realizado una evaluación exhaustiva de la información disponible sobre seguridad, eficacia y calidad de fabricación”.
Acerca de la vacuna de Pfizer contra el coronavirus
La vacuna de Pfizer contiene ARN mensajero, que es un material genético. Contiene una pequeña parte del ARNm del virus SARS-CoV-2. Esta instruye a las células del cuerpo humano la producción de la proteína de pico distintiva del virus en particular. Al momento de recibir esta vacuna, el cuerpo de una persona produce copias de la proteína de pico que no causa la enfermedad. Lo que hace es que el sistema inmune aprenda a reaccionar a la defensiva. De esta manera, se logra la respuesta inmunitaria buscada.
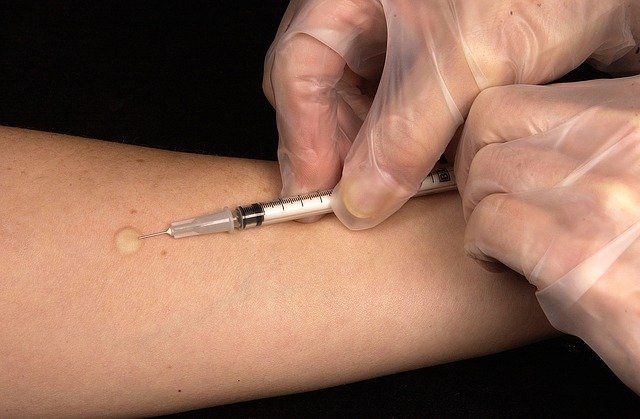
Es una vacuna que se administra en dos dosis, con tres semanas de diferencia entre una y otra. Los datos de seguridad incluyen a 37.586 participantes de los estudios aleatorios. La mayor parte de estos son participantes de Estados Unidos. De ellos, la mitad han recibido la vacuna y la otra mitad un placebo con solución salina. Estos fueron seguidos durante dos meses aproximadamente, luego de recibir una segunda dosis. Los efectos secundarios notificados con más frecuencia incluyen dolor en la zona de la inyección, dolor de cabeza, cansancio, dolor muscular, escalofríos y dolor en articulaciones. En ocasiones, también fiebre.
Conclusiones

Peter Marks, director del Centro de Evaluación e Investigación de Productos Biológicos de la FDA explica que:
“Si bien no es una aprobación de la FDA, la autorización de uso de emergencia de hoy de la vacuna Pfizer-BioNTech COVID-19 promete alterar el curso de esta pandemia en los Estados Unidos (…) Con la ciencia guiando nuestra toma de decisiones, los datos de seguridad y efectividad disponibles respaldan la autorización de la vacuna Pfizer-BioNTech COVID-19 porque los beneficios conocidos y potenciales de la vacuna superan claramente sus riesgos conocidos y potenciales. Los datos proporcionados por el patrocinador han cumplido con las expectativas de la FDA como se transmite en nuestros documentos de orientación de junio y octubre. Los esfuerzos para acelerar el desarrollo de vacunas no han sacrificado los estándares científicos ni la integridad de nuestro proceso de evaluación de vacunas. El proceso de revisión de la FDA también incluyó una revisión pública e independiente de miembros del Comité Asesor de Vacunas y Productos Biológicos Relacionados de la agencia. El logro de hoy es, en última instancia, un testimonio del compromiso de nuestros científicos y médicos profesionales, que trabajaron incansablemente para evaluar a fondo los datos y la información de esta vacuna».







Comment here