El medicamento Avifavir es un tratamiento experimental. Recientemente, el Instituto de Salud Pública (ISP) de Chile ha emitido informaciones respecto al uso de este tratamiento. Para recordar, en el mes de agosto del año 2020, el ISP autorizó la importación de 250.000 comprimidos de Avifavir, lo cual es equivalente a unos 2.500 tratamientos aproximadamente. Ello fue realizado para fines experimentales.
Origen del medicamento Avifavir

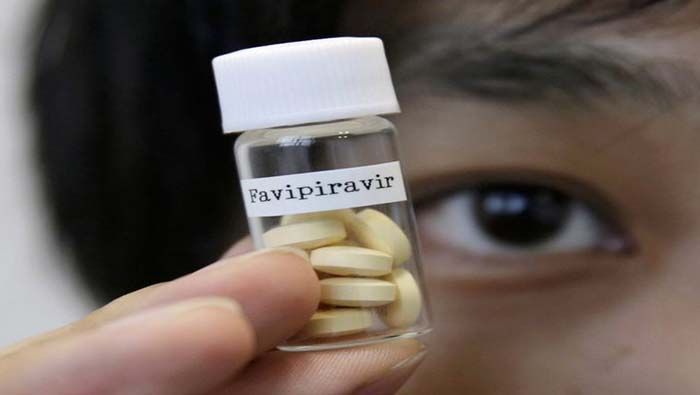
Avifavir es un producto farmacéutico que proviene de Chemical Diversity Research Institute, en Moscú, Rusia. Su principio activo es Favipiravir. Lo que hizo el ISP fue responder a la solicitud de la Asociación Chilena de Municipalidades con Farmacia Popular para la importación de este medicamento en comprimidos recubiertos de 200 mg. Ello, amparándose en el artículo 99 del Código Sanitario. Según este artículo, se permite autorizar provisionalmente tanto la distribución como la venta y el uso de productos farmacéuticos que no cuentan con registro en el país.
Heriberto García, director del ISP, sostuvo que:
“El uso de este medicamento es controlado, es decir sólo se puede utilizar de manera clínica en el Servicio de Atención Primaria de Urgencia de Alta Resolutividad de la comuna de Recoleta, no se vende en farmacias. El ISP lo autorizó excepcionalmente y estará fiscalizando el buen uso, así como también, una posible publicidad indebida (…) Este medicamento no reemplaza a las vacunas, ya que éstas son preventivas para la población, y en caso de que una persona contraiga el COVID-19, la inmunización evita casos graves y reduce las hospitalizaciones. Favipiravir está en periodo de prueba todavía en el mundo y en Chile está autorizado para uso excepcional de manera clínica en personas que ya contrajeron el COVID-19”.
Aclaraciones sobre Avifavir

La solicitud de importación establece que el producto será utilizado en el Servicio de Atención Primaria de Urgencia de Alta Resolutividad de la Comuna de Recoleta. Ello, bajo responsabilidad del Director Médico, que es la persona que debe encargarse de llevar a cabo el correcto seguimiento de los pacientes, reportando cualquier sospecha de reacciones adversas a su utilización en personas.
El ISP ha aclarado que el medicamento Avifavir no puede ser utilizado en mujeres embarazadas. Esto se debe a que puede provocar Teratogénesis. Además, no se puede emplear en pacientes que tienen riesgo de producir la enfermedad de la Gota, debido a la producción de ácido úrico.
Aclara el ISP que la autoridad de salud tiene la capacidad de suspender la distribución si se observa una administración inadecuada. También en caso de verse reacciones adversas severas, como puede ser el caso de una hospitalización asociada a su uso.







Comment here